- Plateforme
Biophysique & Biologie Structurale (B2S)
- Microcalorimétrie, Dichroïsme circulaire, Résonnance plasmonique de surface, RMN, Chromatographie, Diffusion de lumière, Cinétiques rapides, Cryomicroscopie
La plateforme de Biophysique et Biologie Structurale (B2S) offre une combinaison d’équipements destinés à la caractérisation physicochimique in vitro des protéines et des interactions. Elle donne accès à plusieurs équipements de biophysique (dichroisme circulaire, microcalorimétrie, résonance plasmonique de surface, fluorescence) et de biologie structurale (RMN, RX), et s’appuie sur les compétences des équipes de recherche de l’UMR7365 IMoPA. Elle fait partie de l’association ARBRE (Association of Resources for Biophysical Research in Europe) créée en 2015. Depuis 2019, elle est labellisée Structure d'appui à la Recherche (StAR-LUE) dans le cadre du programme INFRA+ de Lorraine Université d'Excellence.
Elle permet le développement de projets pluridisciplinaires en vue de caractériser 1) les interactions mises en jeu entre macromolécules biologiques et, 2) la structure 3D de macromolécules biologiques.
Le personnel de B2S possède un véritable savoir-faire technique et méthodologique permettant d’aborder différentes problématiques : La stabilité/caractérisation des protéines et complexes en solution, la structure tridimensionnelle des protéines et complexes, les cinétiques rapides, la caractérisation des interactions protéine-protéine et protéine-ligand ainsi que l’isolement et la caractérisation d’un large spectre de produits par chromatographie liquide.
La plateforme fonctionne selon deux modes : 1) le mode service (prestations clés en mains dans le cadre, ou non, de collaborations) et 2) le mode mise à disposition d’appareils pour les utilisateurs expérimentés après une formation initiale.
Tout nouveau collaborateur doit contacter le responsable afin de définir la meilleure stratégie à adopter pour la conduite de l’étude. Tout utilisateur s’engagera à accepter les conditions générales et à suivre les consignes d’utilisation.
Nous sommes disponibles pour les utilisateurs pendant toute la durée d’utilisation des appareils et pour tous conseils et assistance.
Chaque utilisateur doit récupérer ses données en fin d’analyse. Dans le cas général, les données brutes d’acquisition sont conservées pendant 1 an sur les postes informatiques. La plateforme ne garantit pas la récupération des données en cas de dysfonctionnement. L’utilisateur est responsable de l’archivage final.
Giraud T , Bouguet-Bonnet S , Marchal P , Pickaert G , Averlant-Petit MC , Stefan L. Improving and fine-tuning the properties of peptide-based hydrogels via incorporation of peptide nucleic acids. Nanoscale. 2020 Oct 14;12(38):19905-19917.
 10.1039/d0nr03483e ,
10.1039/d0nr03483e ,  32985645
32985645 Albe Slabi S, Mathe C, Basselin M, Fournier F, Aymes A, Bianeis M, Galet O, Kapel R. Optimization of sunflower albumin extraction from oleaginous meal and characterization of their structure and properties. Food Hydrocolloids, Volume 99, 2020 Feb, 105335.
 10.1016/j.foodhyd.2019.105335
10.1016/j.foodhyd.2019.105335 - Risser F, Collin S, Dos Santos-Morais R, Gruez A, Chagot B, Weissman KJ. Towards improved understanding of intersubunit interactions in modular polyketide biosynthesis: docking in the enacyloxin IIa polyketide synthase. J Struct Biol. 2020 Jul 25.
 10.1016/j.jsb.2020.107581 ,
10.1016/j.jsb.2020.107581 ,  32717326
32717326 Roret T, Alloing G, Girardet JM, Perrot T, Dhalleine T, Couturier J, Frendo P, Didierjean C, Rouhier N. Sinorhizobium meliloti YrbA binds divalent metal cations using two conserved histidines. Biosci Rep. 2020 Oct 30 ; 40(10):BSR20202956.
 10.1042/BSR20202956 ,
10.1042/BSR20202956 ,  32970113
32970113 Rzeigui M, Traikia M, Jouffret L, Kriznik A, Khiari J, Roy O, Taillefumier C. Strengthening Peptoid Helicity through Sequence Site-Specific Positioning of Amide Cis-Inducing NtBu monomers. J Org Chem. 2019 Dec 24.
 10.1021/acs.joc.9b02916 ,
10.1021/acs.joc.9b02916 ,  31873018 ,
31873018 ,  HAL-02430577
HAL-02430577 Ioannou I, Kriznik A, Chekir L, Ghoul M. Effect of the Processing Temperature on the Degradation of Food Flavonoids: Kinetic and Calorimetric Studies on Model Solutions. J. Food Eng. and Technol. 2019 ; 8(2):91-102.
 10.32732/jfet.2019.8.2.91 ,
10.32732/jfet.2019.8.2.91 ,  HAL-02392716
HAL-02392716 Chagot ME, Dos Santos Morais R, Dermouche S, Lefebvre D, Manival X, Chipot C, Dehez F, Quinternet M. Binding properties of the quaternary assembly protein SPAG1. Biochem J. 2019 May 22.
 10.1042/BCJ20190198 ,
10.1042/BCJ20190198 ,  31118266 ,
31118266 ,  HAL-02140524
HAL-02140524 S Ahmed Zennia S, Mati A, Charron C, Cakir-Kiefer C, Kriznik A, Girardet JM. Effect of nonenzymatic deamidation on the structure stability of Camelus dromedarius alpha-lactalbumin.Food Chemistry. 2019 Avril 8.
 10.1016/j.foodchem.2019.04.033 ,
10.1016/j.foodchem.2019.04.033 ,  HAL-02095313
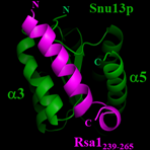
HAL-02095313 Chagot ME, Quinternet M, Rothé B, Charpentier B, Coutant J, Manival X, Lebars I. The yeast C/D box snoRNA U14 adopts a "weak" K-turn like conformation recognized by the Snu13 core protein in solution. Biochimie. 2019 Mar 23.
 10.1016/j.biochi.2019.03.014 ,
10.1016/j.biochi.2019.03.014 ,  30914254 ,
30914254 ,  HAL-02082477
HAL-02082477 Rahuel-Clermont S, Bchini R, Barbe S, Boutserin S, André I, Talfournier F. Enzyme Active Site Loop Revealed as a Gatekeeper for Cofactor Flip by Targeted Molecular Dynamics Simulations and FRET-Based Kinetics. ACS Catal. 2019 ; 9 ; 1337−1346.
 10.1021/acscatal.8b03951 ,
10.1021/acscatal.8b03951 ,  HAL-02022828
HAL-02022828