- Plateforme
Biophysique & Biologie Structurale (B2S)
- Microcalorimétrie, Dichroïsme circulaire, Résonnance plasmonique de surface, RMN, Chromatographie, Diffusion de lumière, Cinétiques rapides, Cryomicroscopie
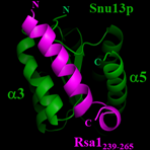
La plateforme de Biophysique et Biologie Structurale (B2S) offre une combinaison d’équipements destinés à la caractérisation physicochimique in vitro des protéines et des interactions. Elle donne accès à plusieurs équipements de biophysique (dichroisme circulaire, microcalorimétrie, résonance plasmonique de surface, fluorescence) et de biologie structurale (RMN, RX), et s’appuie sur les compétences des équipes de recherche de l’UMR7365 IMoPA. Elle fait partie de l’association ARBRE (Association of Resources for Biophysical Research in Europe) créée en 2015. Depuis 2019, elle est labellisée Structure d'appui à la Recherche (StAR-LUE) dans le cadre du programme INFRA+ de Lorraine Université d'Excellence.
Elle permet le développement de projets pluridisciplinaires en vue de caractériser 1) les interactions mises en jeu entre macromolécules biologiques et, 2) la structure 3D de macromolécules biologiques.
Le personnel de B2S possède un véritable savoir-faire technique et méthodologique permettant d’aborder différentes problématiques : La stabilité/caractérisation des protéines et complexes en solution, la structure tridimensionnelle des protéines et complexes, les cinétiques rapides, la caractérisation des interactions protéine-protéine et protéine-ligand ainsi que l’isolement et la caractérisation d’un large spectre de produits par chromatographie liquide.
La plateforme fonctionne selon deux modes : 1) le mode service (prestations clés en mains dans le cadre, ou non, de collaborations) et 2) le mode mise à disposition d’appareils pour les utilisateurs expérimentés après une formation initiale.
Tout nouveau collaborateur doit contacter le responsable afin de définir la meilleure stratégie à adopter pour la conduite de l’étude. Tout utilisateur s’engagera à accepter les conditions générales et à suivre les consignes d’utilisation.
Nous sommes disponibles pour les utilisateurs pendant toute la durée d’utilisation des appareils et pour tous conseils et assistance.
Chaque utilisateur doit récupérer ses données en fin d’analyse. Dans le cas général, les données brutes d’acquisition sont conservées pendant 1 an sur les postes informatiques. La plateforme ne garantit pas la récupération des données en cas de dysfonctionnement. L’utilisateur est responsable de l’archivage final.
de Guillen K, Lorrain C, Tsan P, Barthe P, Petre B, Saveleva N, Rouhier N, Duplessis S, Padilla A, Hecker A. Structural genomics applied to the rust fungus Melampsora larici-populina reveals two candidate effector proteins adopting cystine knot and NTF2-like protein folds. Sci Rep. 2019;9(1):18084.
 10.1038/s41598-019-53816-9 ,
10.1038/s41598-019-53816-9 ,  PMC6889267
PMC6889267 Canabady-Rochelle LLS, Selmeczi K, Collin S, Pasc A, Muhr L, Boschi-Muller S. SPR screening of metal chelating peptides in a hydrolysate for their antioxidant properties. Food Chem. 2018 Jan 15 ; 239:478-485.
 10.1016/j.foodchem.2017.06.116 ,
10.1016/j.foodchem.2017.06.116 ,  28873593 ,
28873593 ,  HAL-01620268
HAL-01620268 Lec J.C, Boutserin S, Mazon H, Mulliert G, Boschi-Muller S, Talfournier F. Unraveling the Mechanism of Cysteine Persulfide Formation Catalyzed by 3-Mercaptopyruvate Sulfurtransferases. ACS Catal. 2018 ; 8(3):2049–2059.
 10.1021/acscatal.7b02432 ,
10.1021/acscatal.7b02432 ,  HAL-01715178
HAL-01715178 Carrasco K, Boufenzer A, Jolly L, Le Cordier H, Wang G, Heck AJ, Cerwenka A, Vinolo E, Nazabal A, Kriznik A, Launay P, Gibot S, Derive M. TREM-1 multimerization is essential for its activation on monocytes and neutrophils. Cell Mol Immunol. 2018 Mar 22.
 10.1038/s41423-018-0003-5 ,
10.1038/s41423-018-0003-5 ,  29568119 ,
29568119 ,  HAL-01945617
HAL-01945617 Bragantini B, Rouillon C, Charpentier B, Manival X, Quinternet M. NMR assignment and solution structure of the external DII domain of the yeast Rvb2 protein. Biomol NMR Assign. 2018 Oct ; 12(2):243-247.
 10.1007/s12104-018-9816-5 ,
10.1007/s12104-018-9816-5 ,  29569106 ,
29569106 ,  HAL-01882005
HAL-01882005 Maurizy C, Quinternet M, Abel Y, Verheggen C, Santo PE, Bourguet M, Paiva A, Bragantini B, Chagot ME, Robert MC, Abeza C, Fabre P, Fort P, Vandermoere F,Sousa P Rain JC, Charpentier B, Cianférani S, Bandeiras TM, Pradet-Balade B, Manival X, Bertrand E. The RPAP3-Cterminal domain identifies R2TP-like quaternary chaperones. Nat Commun. 2018 May 29 ; 9(1):2093.
 10.1038/s41467-018-04431-1 ,
10.1038/s41467-018-04431-1 ,  29844425 ,
29844425 ,  HAL-01872981
HAL-01872981 Henri J, Chagot ME, Bourguet M, Abel Y, Terral G, Maurizy C, Aigueperse C, Georgescauld F, Vandermoere F, Saint-Fort R, Behm-Ansmant I, Charpentier B, Pradet-Balade B, Verheggen C, Bertrand E, Meyer P, Cianférani S, Manival X, Quinternet M. Deep Structural Analysis of RPAP3 and PIH1D1, Two Components of the HSP90 Co-chaperone R2TP Complex. Structure. 2018 Sep 4 ; 26(9):1196-1209.
 10.1016/j.str.2018.06.002 ,
10.1016/j.str.2018.06.002 ,  30033218 ,
30033218 ,  HAL-01919243
HAL-01919243 Kriznik A, Yéléhé-Okouma M, Lec JC, Groshenry G, Le Cordier H, Charron C, Quinternet M, Mazon H, Talfournier F, Boschi-Muller S, Jouzeau JY, Reboul P. CRDSAT Generated by pCARGHO: A New Efficient Lectin-Based Affinity Tag Method for Safe, Simple, and Low-Cost Protein Purification. Biotechnol J. 2018 Oct 8:e1800214.
 10.1002/biot.201800214 ,
10.1002/biot.201800214 ,  30298550 ,
30298550 ,  HAL-01892441
HAL-01892441 Yakavets I, Lassalle HP, Yankovsky I, Ingrosso F, Monari A, Bezdetnaya L, Zorin V. Evaluation of temoporfin affinity to beta-cyclodextrins assuming self-aggregation. Journal of Photochemistry and Photobiology A: Chemistry. 2018 Dec 1.
 10.1016/j.jphotochem.2018.07.046
10.1016/j.jphotochem.2018.07.046 Dorival J, Risser F, Jacob C, Collin S, Dräger G, Paris C, Chagot B, Kirschning A, Gruez A, Weissman KJ. Insights into a dual function amide oxidase/macrocyclase from lankacidin biosynthesis. Nat Commun. 2018 Sep 28 ; 9(1):3998.
 10.1038/s41467-018-06323-w ,
10.1038/s41467-018-06323-w ,  30266997 ,
30266997 ,  HAL-01980537
HAL-01980537